尖端醫新冠試劑 通過國醫預醫所驗證
國際新冠肺炎疫情未見緩,美國當地 Quidel和Becton Dickinson & Co.兩家公司獲得聯邦政府緊急許可,可生產快速篩檢抗原(antigen)試劑組,供給極度吃緊。南韓生技藥廠 Celltrion 也相準機會,準備在美國開賣篩劑的同時,尖端醫經過近二個月的努力,通過國防醫學院預醫所對產品性能的比對確認。
尖端醫分享新冠病毒抗原快篩試劑研發成果,董事長蘇文龍表示,通過國防醫學院預醫所臨床前試驗,對SARS-CoV-2病毒高度辨識性是這產品特色,約需15分鐘可測出結果,其專一性、準確度試紙的穩定性都符合預期,操作上只要從上呼吸道採檢體,混合檢測液,再滴入快篩試劑,就能找出檢體中含有病毒的病患。
尖端醫以生物技術開發中心(DCB)廿年來的ELISA 與快篩試紙平台開發經驗,轉植到新冠病毒檢測相關產品;我們不求快,而是求穩;小心求證與多項的實驗與臨床證實,才是公司首要目標。
判讀方式跟驗孕試劑一樣,陽性有兩條紅線,適合運用於防疫第一線,特別是境外移入或防治社區交叉感染的擴大篩檢之用,且一般醫事人員就可操作,並不需特殊儀器,採用「抗原檢測」,檢測體內是否含有新冠病毒的抗原,能找出檢體中含有病毒的病患,只要15分鐘就能有結果,所以高專一性、快速、準確度高,這些都是快篩試劑一大競爭利基。
尖端醫與國防醫學院預醫所、國家衛生研究院等單位的合作,除了研發量能,也做好量產準備,未來將依防疫實際需求啟動量產。
蘇文龍董事長談到,過往快篩試劑的研發一般至少需要6個月~1.5年的時間,尖端醫團隊在6月上旬投注全部研發人力、物力等資源下,進而縮短研發流程。
尖端醫食安快篩試劑市場,國內市佔率最高,該公司將在衛福部緊急授權專案製造核准後,準備好隨時進入量產,此時,新的GMP規格體外檢測試劑廠也預期在九月底完工,將正式進軍體外檢測試劑,並逐步提升至最高產能,以供國內、外防疫需求。在新冠病毒蔓延全球,依中央流行疫情指揮中心(24)日監測資料顯示,COVID-19(武漢肺炎) 全球確定病例數逾2341萬人確診,分布於187個國家/地區,在防疫物資大缺貨,檢測試劑需求更是強勁下,讓尖端醫的檢測試劑被期待值水漲船高,更吸引不少國外廠商洽談合作中。
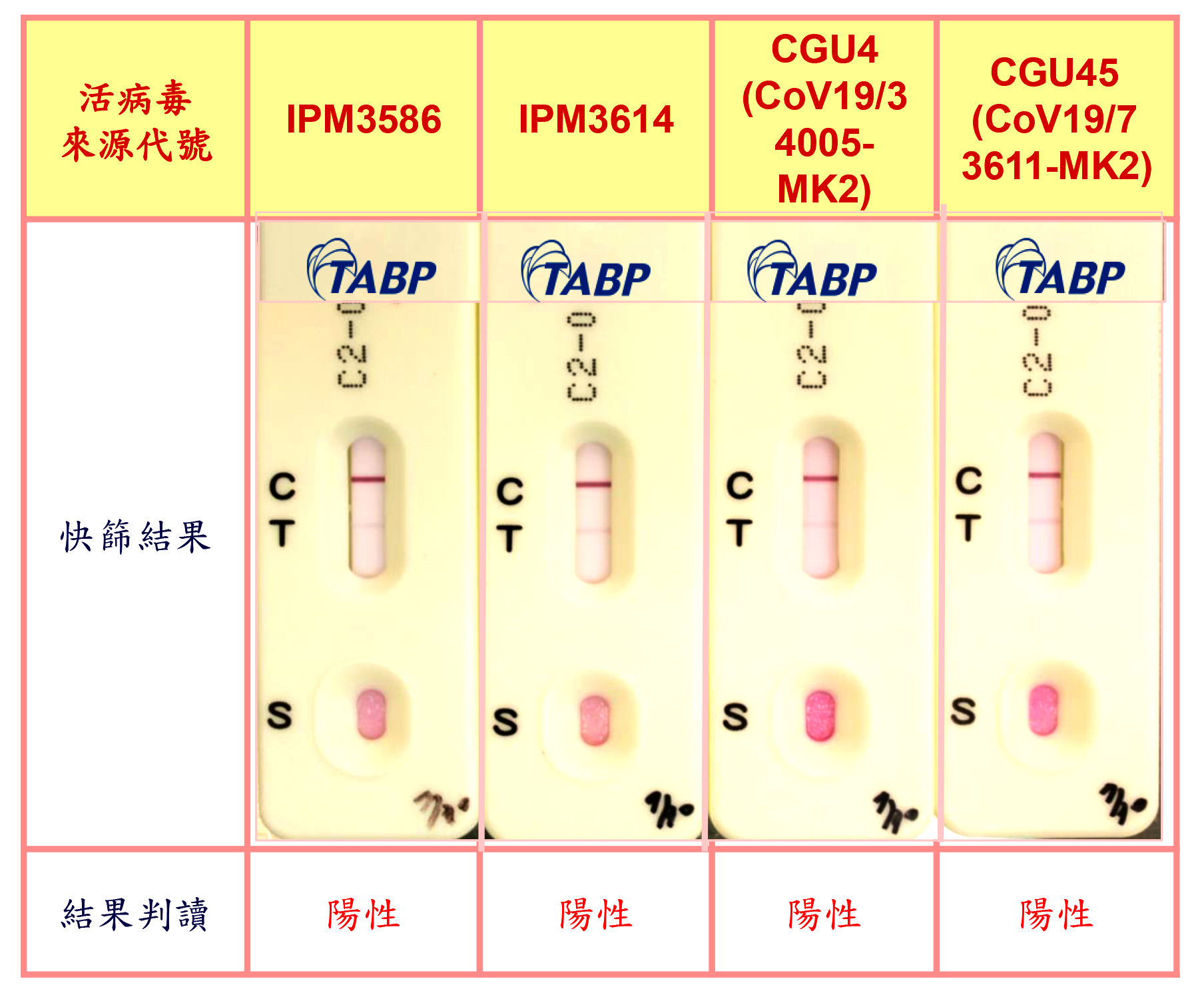
尖端醫技轉國醫預醫所及國衛院快篩原料後,與預醫所合作進行試劑性能評估實驗,目前已可辨認不同來源的新冠肺炎活病毒,本月將進行臨床試驗申請。圖為預醫所驗證測試結果。


